近日,《Advanced Science》在线发表了金沙集团1862cc/金沙集团1862cc纳米酶工程实验室高利增课题组的研究论文"Mucosal Vaccination for Influenza Protection Enhanced by Catalytic Immune‐Adjuvant"。该工作提出了以纳米酶作为催化佐剂提高鼻腔粘膜免疫的策略。
流行性感冒是由流感病毒引发的呼吸道传播疾病,历史上每次流感病毒的大流行都给人类健康和社会经济造成巨大损失。目前防控流感最常用的策略是肌肉注射流感病毒灭活疫苗。但肌肉注射途径的疫苗难以在黏膜部位诱导特异性SIgA黏膜抗体以有效阻断病毒的入侵和散播。鼻腔是流感病毒进入宿主的主要入口,如果在鼻腔和上呼吸道建立有效的黏膜免疫保护,将有效阻止流感病毒的早期入侵。但是目前存在的关键问题是流感病毒疫苗较难突破黏膜屏障的阻挡,难以通过鼻腔粘膜诱导有效的免疫应答。
针对该问题,研究人员基于氧化铁纳米酶(Iron oxide nanozyme, IONzyme)的催化特性,提出了"催化免疫佐剂"新策略。氧化铁纳米酶是2007年高利增博士在阎锡蕴课题组首次发现的具有类过氧化物酶活性的一类经典纳米酶(Nature Nanotechnology 2007),该课题组多年来紧密围绕氧化铁纳米酶的设计、催化机制和生物医学应用展开研究,将其拓展用于体外诊断、肿瘤诊疗、抗菌/抗病毒(Biomaterials 2016, Theranostics 2017/2019, Nature Communications 2018)等多个领域。在上述研究基础上,研究人员提出了基于氧化铁纳米酶增强流感病毒疫苗鼻腔粘膜免疫的策略,一方面利用纳米酶作为载体突破黏膜屏障实现灭活流感病毒疫苗的高效递送;另一方面利用纳米酶调控ROS的特性诱导高水平的黏膜免疫应答,最终提高疫苗免疫效果。
首先,研究人员在氧化铁纳米酶表面修饰一定比例的壳聚糖,在提高催化活性的同时,让纳米酶表面携带大量正电荷。修饰后的纳米酶与负电性的流感病毒颗粒结合,形成纳米酶/灭活流感病毒复合体,同时可在负电性的鼻腔上皮表面粘附,从而显著提高疫苗的黏膜靶向递送效率。进一步研究发现纳米酶能够激活黏膜上皮细胞TLR2/4受体通路,促进趋化因子CCL20的分泌,快速招募DC细胞迁移至黏膜下区域跨上皮摄取鼻腔流感抗原。复合体被DC细胞捕获后,纳米酶可在溶酶体酸性环境下发挥过氧化物酶活性,显著提高ROS水平促进树突状细胞成熟分化,并进一步激活下游一系列天然免疫应答。同时,DC细胞迅速向附近引流淋巴结-颈淋巴结迁移,将加工处理的流感抗原向T淋巴细胞递呈,诱导高水平的IgA黏膜免疫应答和IgG系统性免疫应答。动物免疫和攻毒试验结果表明,该纳米酶/灭活流感病毒复合体两次滴鼻免疫可完全保护小鼠对H1N1流感病毒的致死性攻击。此外,氧化铁纳米酶具有生物稳定性好、成本低、生物安全性高等特点,因此有可能作为佐剂广泛应用于新型黏膜疫苗的研发。
该工作由金沙集团1862cc和扬州大学合作完成,扬州大学青年教师秦涛及研究生马尚为共同第一作者,金沙集团1862cc高利增、扬州大学阴银燕及彭大新为共同通讯作者。该研究得到国家重点研发计划、国家自然科学基金等项目的资助。
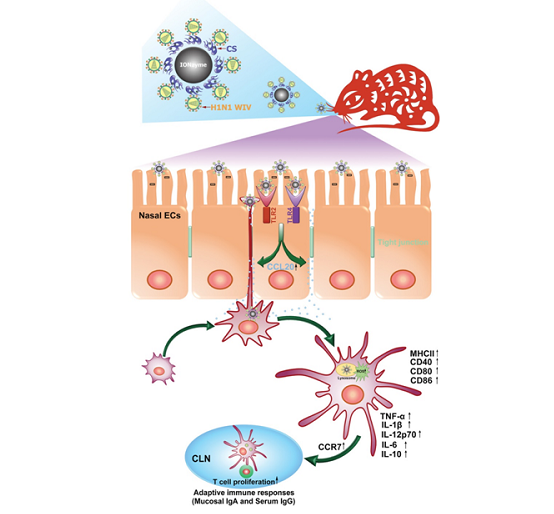
纳米酶作为催化佐剂提高流感病毒鼻腔粘膜免疫效果示意图
文章链接:https://doi.org/10.1002/advs.202000771
(供稿:高利增研究组)
