如果把人体比作社会,身体内的每个细胞就好像社会中的成员。为了维护“社会”的和谐稳定,每个体细胞成员都各司其职,它们被训练得高度“专业”,以适应自己的功能。相对于这些成熟的体细胞,干细胞倒像是未接受过任何专业训练的学生。具有从事各种职业的潜能,比如修复损伤组织、替代损伤细胞的功能或刺激机体自身细胞的再生。干细胞的这种特性被应用于治疗多种人类退行性和损伤性疾病。例如:通过人为控制干细胞的分化,可修复或替换那些受损和“即将退休”的组织细胞,用于治疗心肌梗死、糖尿病、神经退行性疾病等多种疾病。
干细胞技术在再生医学中具有广阔的应用前景,但有效性和安全性方面的局限性阻碍了该技术的普及。一方面,注入体内的干细胞在疾病以及衰老微环境下存活效率不高;另一方面,不利因素的刺激可能导致干细胞的基因组不稳定而突变成肿瘤细胞,在细胞治疗中形成安全隐患。
至此,大家可能会想到,如果让移植入体内的干细胞能够更好地适应非正常生理状况下的不良微环境,是不是就有可能跨越“有效性”和“安全性”这两大障碍?
为了实现到上述目标,金沙集团1862cc刘光慧研究组、北京大学汤富酬研究组和金沙集团1862cc动物研究所曲静研究组联合攻关,通过靶向编辑单个长寿基因产生了世界上首例遗传增强的人类血管细胞,在解决细胞治疗的“有效性”和“安全性”这两大难题上实现了突破。
此次靶向编辑的基因是名为“FOXO3”的转录因子,由于FOXO3的基因多态性同人类寿命的延长关系密切,因此被冠以“长寿蛋白”的美名。它通过调节多种基因表达,可实现延缓细胞衰老、抵御应激、维持心血管稳态等作用。此外,FOXO3还具有抵抗肿瘤形成的能力。
刘光慧领导的团队在人类干细胞中利用基因编辑技术成功做到了使FOXO3蛋白在细胞核里“停留”更长的时间,从而更好地发挥作用。随后,研究人员将这种被成功编辑的干细胞分别分化成血管内皮细胞(血管内膜)、血管平滑肌细胞(血管中膜)和间质细胞(血管外膜)。这些血管细胞就像是增强了装备的士兵,既提高了战斗力,又可以适应“战场”中恶劣的环境,随时准备增援体内老化损伤的细胞。
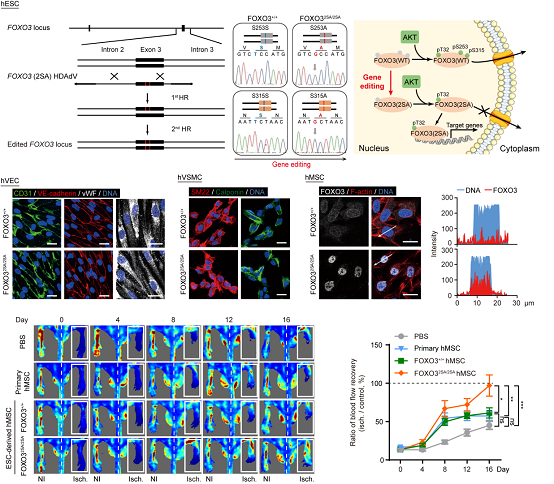
图1. 通过基因编辑产生FOXO3功能增强的人类血管细胞,用于治疗缺血性血管病变
当将“增强”的细胞移植到小鼠发生缺血性损伤的后肢中时,可高效促进受损血管的再生,加速恢复缺血部位的血流,证明FOXO3功能增强的人类血管细胞具有明显优于野生型细胞的血管修复能力。在机制方面,内源激活的FOXO3通过拮抗CSRP1基因表达介导对血管细胞衰老的抵抗作用。
为验证遗传增强干细胞作为移植材料的安全性,研究人员为它们设计了一种极端环境:将多种致癌因子导入野生型和FOXO3功能增强的胚胎干细胞中。结果发现,遗传增强干细胞还可以有效地抵抗癌基因诱导的细胞恶性转化。
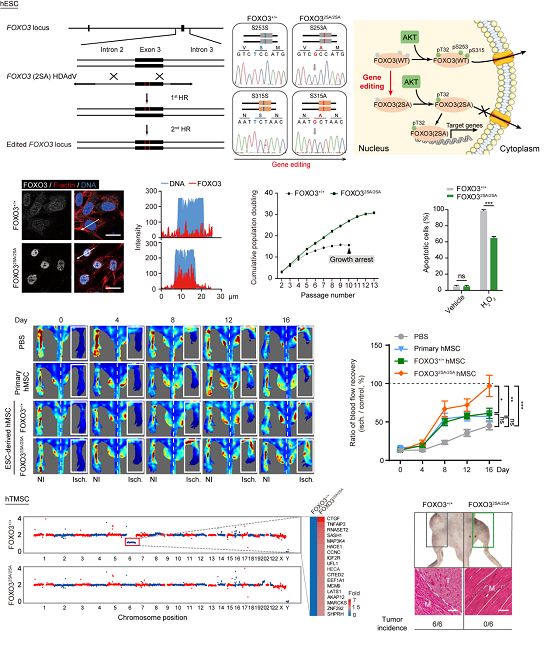
图2. FOXO3增强型人血管细胞对细胞癌化具有强抵抗作用。
刘光慧等研究组首次利用基因编辑技术获得了FOXO3功能增强的人类血管细胞,实现了细胞治疗中“有效性”和“安全性”的突破,从概念上证明了利用基因编辑策略获得优质安全人类血管细胞移植物的可行性。为未来的再生医学提供了一个具有潜力的选项,对发展更加安全有效的临床细胞治疗策略具有深远意义。
(作者:刘光慧)
 附件下载:
附件下载: