衣康酸的初发现
许多读者可能对衣康酸感到陌生。其实,最早的衣康酸研究可追溯到19世纪30年代。从分子结构角度看,衣康酸(C5H6O4)是一种不饱和二元羧酸,又被称为2-亚甲基丁二酸或2-亚甲基琥珀酸(图1a)。早在1836年,瑞士药剂师Samuel Baup在研究柠檬酸的热分解反应时发现了一种未知化合物,即衣康酸[1]。1840年,德国学者Gustav Crasso确认了衣康酸是顺乌头酸热分解反应的产物,他将顺乌头酸(aconitate)的英文字母顺序重新排列并命名该产物为衣康酸(itaconate)[2]。当时的科学家可能没有意识到衣康酸潜在的工业应用价值,并没有对其进行更深入地研究。直到1931年,日本学者Kinoshita K才首次报道利用衣康酸曲霉(Aspergillus itaconicus)生产衣康酸[3]。后来科学家们又陆续发现包括土曲霉在内的多种菌株都能够用于生产衣康酸。
目前,衣康酸的生产方法主要有化学合成法和发酵法。由于衣康酸化学性质活泼,可参与各种加成反应、聚合反应及酯化反应,所以它是一种重要的有机合成和化工生产原料。其用途也十分广泛,例如用于生产尿不湿、电脑及手机显示屏等(图1b~e)。
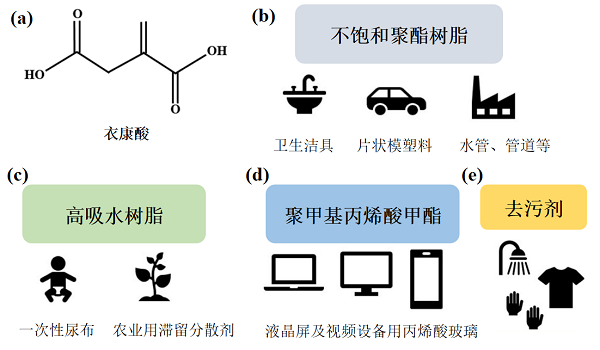
图1. 衣康酸结构式及主要工业用途[4]
(a) 衣康酸(C5H6O4)的结构式,其含有不饱和双键,化学性质活泼。(b~e) 衣康酸是生产不同工业产品的原材料,例如可以生产尿不湿及农业用滞留分散剂;还可以用于生产手机、电脑显示屏等。另外,也能用于制造片状膜塑料、卫生洁具及管道和去污剂等。
衣康酸作为免疫代谢产物的重生之路
从最初的工业应用到重新定义衣康酸的生物学功能,衣康酸的研究可谓取得新突破。近十几年的最新研究揭示了衣康酸是巨噬细胞产生的一种发挥免疫调节功能的三羧酸循环代谢产物。2013年,卢森堡Karsten Hiller研究团队发现由免疫应答基因1 (immunoresponsive gene 1, Irg1) 编码的顺乌头酸脱羧酶负责将处于活化状态巨噬细胞内的顺乌头酸脱羧转化为衣康酸,从而阐明了巨噬细胞内衣康酸的生成途径[5]。在受到脂多糖(LPS)刺激时,巨噬细胞内会诱导产生毫摩尔级别的衣康酸。因此,巨噬细胞内同样存在衣康酸降解通路。简单来讲,1分子衣康酸最终被裂解为1分子乙酰辅酶A和1分子丙酮酸。迄今为止,巨噬细胞及髓系细胞是唯一可被刺激诱导产生衣康酸的细胞类型。
衣康酸的抗炎、抗菌及抗病毒作用
衣康酸在巨噬细胞内主要发挥抗炎功能。作为三羧酸循环产生的代谢产物,衣康酸在线粒体内可抑制琥珀酸脱氢酶的活性,从而减少线粒体活性氧的产生,最终达到减弱炎症反应的效果[6]。另外,衣康酸还能够从线粒体基质穿梭到细胞质中。在细胞质内,衣康酸发挥抗炎功能的主要机制是通过thia-Michael加成反应烷基化修饰相关蛋白质的半胱氨酸残基。例如,通过烷基化修饰KEAP1(Kelch like ECH associated protein 1)蛋白并激活Nrf2信号通路减轻巨噬细胞的炎症反应及氧化应激[7]。
衣康酸还具有抗菌作用。自1977年以来,科学家们就发现衣康酸能够抑制葡萄糖剥夺条件下靛蓝假单胞菌的生长。衣康酸主要通过抑制细菌内异柠檬酸裂解酶的活性,从而阻断细菌生长和致病性所需的乙醛酸分流途径,进而发挥其抗菌作用[8]。另外,衣康酸的中间代谢产物衣康酰辅酶A能抑制细菌内甲基丙二酰辅酶 A 变位酶的活性,继而阻断依赖丙酰辅酶 A的细菌生长,例如结核分歧杆菌[9]。笔者博士后期间研究发现,巨噬细胞在被细菌感染条件下,衣康酸介导的TFEB烷基化修饰诱导巨噬细胞内溶酶体的生物合成,进而增强机体的抗菌先天免疫能力[10](图2)。我们的研究拓展了衣康酸抗炎之外的其他重要生物学功能。
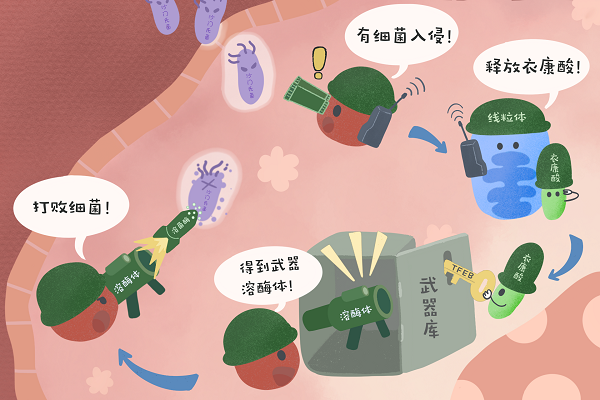
图2. 衣康酸通过诱导溶酶体生物合成来增强机体的抗菌能力
当巨噬细胞发现细菌入侵时,会立即做出响应使线粒体释放衣康酸,衣康酸通过烷基化修饰TFEB激活其入核并促进溶酶体的生物合成,进而消灭入侵的细菌。
有趣的是,衣康酸还表现出抗病毒效果。例如,衣康酸衍生物抑制寨卡病毒、单纯疱疹病毒及牛痘病毒的复制[11]。这提示衣康酸表现出治疗病毒感染的潜力。
总结与展望
自19世纪人们发现衣康酸以来,其主要被用于生产工业制品的原材料。直到近十几年才发现衣康酸存在于哺乳动物巨噬细胞内,而且是具有重要免疫调控功能的代谢产物,这也提示其可作为多种疾病的潜在治疗靶点。衣康酸属于细胞内源产生的代谢产物,利用其作为潜在的药物候选分子,理论上不会引起严重的副作用,这是优势所在。总之,衣康酸可以说是免疫细胞代谢重编程最好的例子之一。
随着对衣康酸研究的不断深入,许多新问题也涌现出来。是否还存在其他可以产生衣康酸的细胞类型未被发现?另外,衣康酸发挥的其他未知生物学功能也值得继续研究。近日,李新建团队开发了一种具有亚细胞分辨率可实时监测衣康酸浓度变化的生物感受器[12],这一创新性工具将极大提高人们解答相关问题的效率。衣康酸或许只是冰山一角,巨噬细胞内衣康酸的同分异构分子——中康酸和柠康酸的发现,暗示或许在不久的将来会涌现出更多的抗炎代谢产物,让我们拭目以待!
参考文献
1. Baup S. Ueber eine neue Pyrogen- Citronensaure, und uber Benennung der Pyrogen- Sauren uberhaupt. Ann Pharm,1836, 19: 29-38
2. Crasso G L. Untersuchungen über das Verhalten der Citronsaure in hoherer Temperatur und die daraus hervorgehenden Produkte. Justus Liebigs Ann Chem, 1840, 34: 53-84
3. Kinoshita K. Uber eine Aspergillus Art, A. itaconicus. Bot Mag Tokyo, 1931, 45(530): 45-61
4. da Cruz J C, de Castro A M, Camporese Servulo E F. World market and biotechnological production of itaconic acid. 3 Biotech, 2018, 8(3): 138
5. Michelucci A, Cordes T, Ghelfi J, et al. Immune-responsive gene 1 protein links metabolism to immunity by catalyzing itaconic acid production. Proc Natl Acad Sci USA, 2013, 110(19): 7820-7825
6. Lampropoulou V, Sergushichev A, Bambouskova M, et al. Itaconate links inhibition of succinate dehydrogenase with macrophage metabolic remodeling and regulation of inflammation. Cell Metab, 2016, 24(1): 158-166
7. Mills E L, Ryan D G, Prag H A, et al. Itaconate is an anti-inflammatory metabolite that activates Nrf2 via alkylation of KEAP1. Nature, 2018, 556(7699): 113-117
8. McFadden B A, Purohit S. Itaconate, an isocitrate lyase-directed inhibitor in Pseudomonas indigofera. J Bacteriol, 1977, 131(1): 136-144
9. Ruetz M, Campanello G C, Pruchal M, et al. Itaconyl-CoA forms a stable biradical in methylmalonyl-CoA mutase and derails its activity and repair. Science, 2019, 366(6465): 589-593
10. Zhang Z, Chen C, Yang F, et al. Itaconate is a lysosomal inducer that promotes antibacterial innate immunity. Mol Cell, 2022, 82(15): 2844-2857.e10
11. Olagnier D, Farahani E, Thyrsted J, et al. SARS-CoV2-mediated suppression of NRF2-signaling reveals potent antiviral and anti-inflammatory activity of 4-octyl-itaconate and dimethyl fumarate. Nat Commun, 2020, 11(1): 4938
12. Sun P, Zhang Z, Wang B, et al. A genetically encoded fluorescent biosensor for detecting itaconate with subcellular resolution in living macrophages. Nat Commun, 2022, 13(1): 6562
作者简介:

张振兴
金沙集团1862cc李新建组助理研究员。研究方向为天然免疫反应中的代谢重编程。
科学寄语
揭秘衣康酸,争做排头兵。
 附件下载:
附件下载: